考生须知:1.答案必须写在答题纸上,写在试卷上无效
2.考试结束后,请将试题连同试卷一起装袋密封
一、 选择题(每小题1分,共35分)
1. 同浓度的下列何种物质对AgI 正溶胶的聚沉能力最强
A. Na2SO4 B.NaNO3 C.K3PO4 D.Al(NO3)3 E.Mg(NO3)2
2. 在其它条件不变的情况下, KMnO4在下列介质中氧化能力最强的是
A.pH=0.0 B.pH=7.0 C.pH=2.0 D.pH=9.0 E.pH=4.0
3. 在滴定实验中不能用所装溶液润洗的仪器是
A. 锥形瓶 B.滴定管 C.移液管 D.小烧杯 E.量筒
4. 属于两性物质的是
A. CO32- B. H2S C. HCl D. Ac- E.H2PO4-
5.冰在100kPa,0℃时融化,下列选项正确的是
A. ΔU=0 B. ΔH=0 C. ΔG=0 D. ΔS=0 E.以上答案都不对
6.摩尔燃烧热为”0”的物质是
A. CH4(g) B. N2(g) C.CH3OH(g) D. CO(g) E.C2H4(g)
7.不能形成氢键的分子是
A.H2O B.H3BO3 C.NH3 D.HNO3 E.CH4
8.相同浓度的下列溶液pH值最高的是
A.NaAc B.NaCl C.NaCN D.NaNO3 E.Na2SO4
9.错误的原子轨道符号是
A.Pxy B. Pz C. dxy D.dx2 - y2 E. dyz
10.描述3S电子运动状态的量子数正确的一套是
A. (3,2,0,+1/2) B. (3,0,0,-1/2) C.(3,1,0,+1/2) D.(3,1,1,-1/2)
E.(2,1,0,-1/2)
11.下列化合物中既有σ键又有π键的化合物是
A. CH4 B.BF3 C.NH3 D.CH2=CH2 E.BeCl2
12.[Ni(NH3)4]2+的空间构型为正四面体型,Ni2+的外层轨道采取的杂化类型是
A.sp B.sp2 C.sp3 D.dsp2 E.d2sp3
13.实验中正确记录K2MnO4标准溶液的浓度是
A.0.0201 B.0.02010 C.0.020100 D.0.020101 E.0.020
14.如某HB弱酸的Ka=1×10-5,则此弱酸的缓冲系的缓冲容量最大的pH值范围是
A.2~4 B.3~4 C.4~5 D.3.5~4.5 E.4~6
15.下列物质中,哪个分子具有磁性
A .N2 B.O2 C. F2 D. CH4 E. NH3
16.下列配合物中属于螯合物的是
A.[Zn(NH3)4]2+ B. [Cu(NH3)4]2+ C. [Ag(CN)2]- D. [Cu(en)2]2+
E. [Ni(NH3)4]2+
17.某一级反应,开始浓度为8mol/l,100min时的浓度为4mol/l,当反应只剩下1mol/l时共需
A.100min B.175min C.300min D.700min E.400min
18.下列与0.2mol/l葡萄糖互为等渗溶液的是(水的Kf=1.86)
A. 凝固点为0.372℃的NaCl溶液 B. 凝固点为-0.186℃的NaCl溶液 C. 凝固点为-0.186℃的蔗糖溶液
D.凝固点为-0.372℃的NaHCO3溶液 E. 凝固点为3.72℃的CaCl2溶液
19.液态氨分子之间存在的作用力有
A. 色散力 B. 色散力,取向力 C. 色散力,取向力,诱导力 D. 色散力,取向力,诱导力和分子间氢键
E.氢键
20. 可见光的波长范围是
A.200~400nm B.400~760nm C. 200~1000nm D.800~1000nm
E. 200~800nm
21.下列哪个化合物能发生Cannizzaro 反应
A.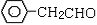 B.
B.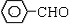 C.CH3CHO D.CH3CH2OH E. (CH3)2CHCHO
C.CH3CHO D.CH3CH2OH E. (CH3)2CHCHO
22.下列哪些糖可以生成相同的糖脎
A. D-果糖, D-葡萄糖, L-甘露糖 B. D-蔗糖, D-麦芽糖, D-纤维二糖
C. D-半乳糖, D-果糖, D-乳糖 D. D-果糖, D-半乳糖, D-葡萄糖 E. D-葡萄糖,
D-甘露糖, D-果糖
23. 下列化合物中, 含有最活泼的氯原子的是
A. C6H5Cl B. 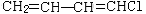 C.
C.
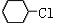 D.
C6H5CH2Cl E. CH3CH2Cl
D.
C6H5CH2Cl E. CH3CH2Cl
24. 卤烷SN1反应速度不取决于试剂的亲核性大小是因为
A. 亲核试剂的亲核性差别很小 B. 亲核试剂始终是过量的 C. 亲核试剂是反应过程中各步反应的参加者
D. 亲核试剂并非是第一步慢反应的参加者 E. 亲核试剂只是SN1反应的催化剂
25. 对于氢氧化钠水溶液与溴甲烷之间进行的反应最好说成是
A. 自由基反应 B. 消除反应 C. OH-的亲核进攻 D. Na+的亲电进攻 E. H+的亲电进攻
26. 醇醛缩合反应常用的催化剂是
A. 浓H2SO4 B. 50%NaOH C. 2MH2SO4 D. 干燥HCl E. 5%NaOH
27. 羧酸衍生物的水解、醇解和氨解反应, 其反应机理最确切的提法为
A. 亲核加成 B.亲核取代 C.亲核加成-消去 D.消去反应 E.游离基加成-消去
28. 下列具有还原性的酸是
A. 乙酸 B. 草酸 C. 丁二酸 D. 丙酸 E. 软脂酸
29. 下列化合物中除_______外其余均为具有芳香性的杂环化合物
A. 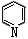 B.
B.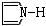 .
C.
.
C. D.
D. 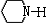 E.
E.
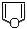
30. 油脂碘值的大小可以标志
A. 活泼性 B. 平均分子量 C. 不饱和度 D. 相对含量 E. 稳定性
31. 加入下列哪一种物质可催化蔗糖转化反应
A. Pt B. Fehling溶液 C. 盐酸 D. 唾液淀粉酶 E. H2
32. 与亚硝酸作用不放出氮气的氨基酸是
A. 色氨酸 B. 组氨酸 C. 赖氨酸 D. 精氨酸 E. 脯氨酸
33. ClCH2CH2Br中最稳定的构象是
A. 顺交叉式 B. 邻位交叉式 C. 部分重叠式 D. 全重叠式 E. 反交叉式
34. α-D-吡喃葡萄糖与β-D-吡喃葡萄糖互为
A. 对映异构体 B. 官能团异构 C. 端基异构体 D.旋光异构体 E.差向异构体
35. 下列乙酰化试剂中活性最强的是
A. 乙酸酐 B. 乙酰胺 C. 乙酰氯 D. 乙酸乙酯 E. N-甲基乙酰胺
二.填空题(每空1分,共计30分)
1. 原子轨道组合成分子轨道的三原则是: ____ ____ _______, ______ __________,
________ __________.
2. 配合物的价键理论认为配体所提供的 电子填入中心 的___________________轨道.
3. 人体血浆中存在的缓冲系主要有_____________,________ , .
4. 价键理论认为两个原子之间只有__________个σ键,余者为__________键;________是化学反应的积极参与者。
5. φ°(Zn2+/Zn)=-0.76V, φ°(Cu2+/Cu)=+0.34V,当他们组成电池时,电池符号可表示为__________________________,电池反应为___________________________,标准状态下的电池电动势为_____________________
6. 对于________反应来说,反应分子数和反应级数是一致的。
7. 系统的混乱度越大,所具有的熵值_______________,系统混乱度的变化叫作_______________。
8. 将等体积的0.9% (g/ml)NaCl和9% (g/ml)KCl溶液用半透膜隔开,水分子的渗透方向是______________________。
9. 由于强电解质溶液中存在着离子氛和离子对,因此常用_______________表示有效浓度
10.D-甘露糖用稀碱溶液处理至少可得到____________、____________和____________几种单糖的混合物。
11. SN1反应历程特点____________分子反应, 反应速度___________浓度有关, 反应是分______步进行的,
活泼中间体为____________。
12. 亲核加成反应首先进攻的离子是_________, 双键中断裂的键是___________键。
13. 自然界的单糖绝大多数都是__________型糖。
三.简答题(每小题6分,30分)
1. 简述胶粒带电的原因.
2. 发生有效碰撞的反应物分子应具有的两个条件是什么?
3. 写出 24Cr的核外电子排布式。
4. 写出O2分子的分子轨道电子排布式,并比较O2与O2+的稳定性.
5. 简述如何配制某一pH值的缓冲溶液.
四.计算题(每小题6分,30分)
1. 已知φ0Ag+/Ag=0.7991V, φ0AgCl/Ag =0.2223V 求Ksp(AgCl)
2. 在100℃时,阿司匹林水解的半衰期为0.0875天,活化能为56.5kJ/mol,求17℃时阿司匹林的水解常数是多少?(设阿司匹林水解为一级反应)
3. 求浓度为0.100mol/L,ka为1.40×10-3的某一元弱酸的pH值。
4. 某溶液含2.5%葡萄糖及0.45%NaCl, 计算此溶液的渗透浓度(mOsmol/l), 已知M葡萄糖=180,MNaCl=58.5.
5. 在1升0.2mol/l的HAc溶液中加入0.1mol/l的固体NaOH(忽略固体NaOH加入引起的体积变化),计算此溶液的pH值?(已知pKb(Ac-)=9.25).
五.写出下列化合物的结构式(每小题1分,共5分)
1. 苦味酸 2.嘌呤 3.麦芽糖(Haworth式)
4.环戊烷并氢化菲 5.(E)―富马酸
六、完成下列反应式(每小题1分,共5分)
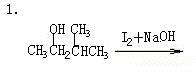
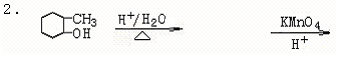
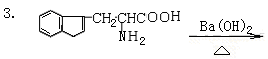
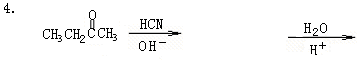
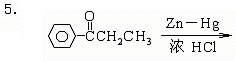
七、合成题(每小题5分,共10分)
1.由乙醇合成丁二酐
2.由苯合成对羟基偶氮苯
八、推测题(每小题5分,共5分)
1.分子式为C9H10O2的化合物(Ⅰ) 能溶于NaOH溶液,易和溴水羟胺反应,和Tollens试剂不作用。经LiAlH4还原则产生化合物(Ⅱ),其分子式为C9H12O2。(Ⅰ)与
(Ⅱ)均有碘仿反应, 用锌汞齐与盐酸还原(Ⅰ)生成分子式为C9H12O的(Ⅲ), 将(Ⅲ)用NaOH反应后再用碘甲烷作用得到化合物(Ⅳ),
(Ⅳ)的分子式为C10H14O, 用KMnO4溶液氧化得对-甲氧基苯甲酸。试写出化合物(Ⅰ)、(Ⅱ)、(Ⅲ)、(Ⅳ)的结构式。




